【
儀表網 研發快訊】可變形液態金屬在生物醫學、柔性電子和微納馬達等領域的應用至關重要。與剛性微納米金屬材料相比,柔性微納米液態金屬擁有更強的順應性和易于調控等特性。在生物醫學領域,常規納米顆粒面臨“尺寸困境”:小尺寸顆粒易于細胞穿透但滯留時間短,大尺寸顆粒雖滯留時間長但難以高效進入細胞。如何實現“既進得去,又留得住”成為納米藥物設計的關鍵難題。
近日,中國科學院理化技術研究所在可變形液態金屬納米顆粒(LMPs)的細胞內外動態行為機制研究中取得重要進展。該研究從理論及實驗層面揭示了液態金屬納米顆粒在腫瘤微環境中的靶向自組裝、細胞內自融合及溶酶體逃逸全鏈條動態作用機制,為新一代智能納米藥物設計提供了新思路(圖1)。
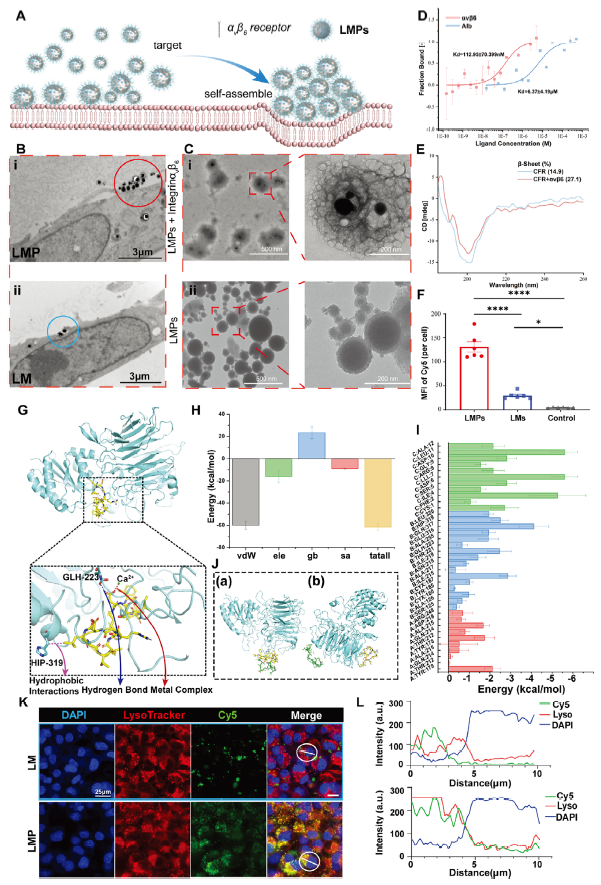
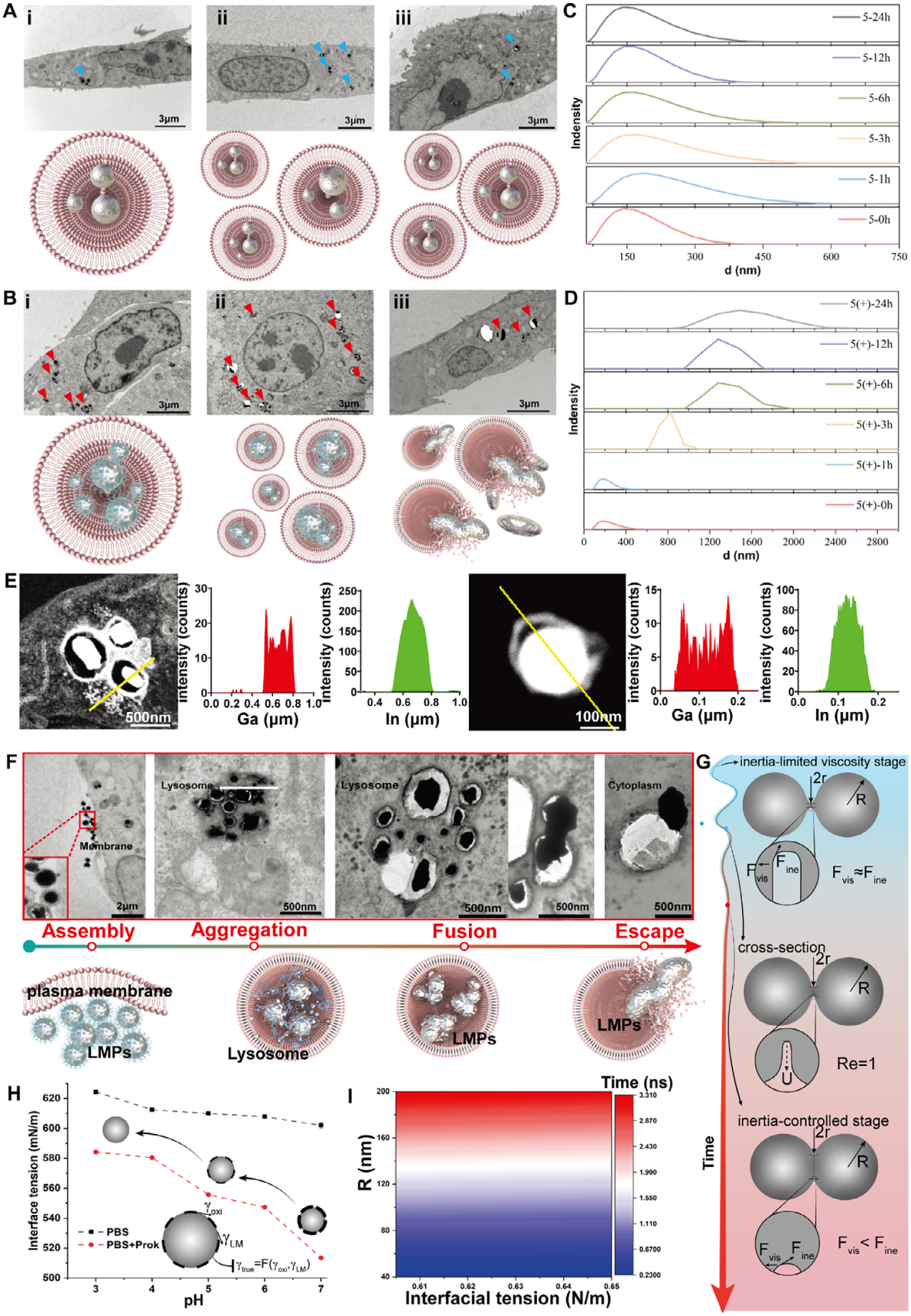
理化所低溫科學與技術全國重點實驗室液態金屬與低溫生物醫學研究中心利用液態金屬材料變形特性與自組裝肽修飾設計,使LMPs具備獨特的“動態變形能力”。在細胞膜層面,可變形液態金屬納米顆粒可實現主動靶向與自組裝,強化了微觀定向傳質效果,顯著提升了腫瘤細胞對其的內吞效率(圖2)。進入溶酶體后,酸性/酶微環境作用使得液態金屬氧化膜逐漸消失從而觸發金屬顆粒的自融合,實現“先小后大”的細胞內尺寸躍遷。研究團隊對該過程進行了深入的數理計算和透射電鏡微觀對比分析,將融合過程劃分為慣性限制粘性階段、過渡階段以及慣性控制階段,為持續線粒體應激與誘導細胞死亡效應放大提供了結構基礎(圖3)。從溶酶體逃逸后,可變形液態金屬顆粒持續釋放的鎵離子進一步介導了線粒體損傷機制,釋放的Ga³?通過鐵替代途徑破壞線粒體鐵硫簇組裝,干擾了線粒體電子傳遞鏈功能,進而觸發免疫原性細胞死亡(圖4)。
更進一步的,結合不可逆電穿孔的破膜技術,LMPs可進一步促進損傷相關分子模式和腫瘤抗原向細胞膜外部釋放,激活樹突狀細胞成熟和記憶性T細胞分化,形成長效抗腫瘤免疫記憶。研究團隊通過復挑戰實驗也驗證了“腫瘤特異性免疫記憶”的建立:聯合治療可誘導更強的腫瘤特異性T細胞反應,并在同源腫瘤再接種中獲得顯著保護;而對異源腫瘤并未表現出同等保護,提示該記憶應答具有抗原特異性。這為“局部治療-系統免疫-長期記憶”的閉環提供了證據支撐,也凸顯了該策略在“原位疫苗化”方向的潛力。
相關研究工作以Liquid Metal Nanoparticles-Mediated Mitochondrial Damage Enhances Immunogenic Cell Death for Cancer Vaccine Therapy為題發表在Advanced Materials。論文第一作者為中國科學院理化技術研究所和北京中醫藥大學聯合培養生戚瑜瑕、于中陽,及中國科學院理化技術研究所研究生張杰,中國科學院理化技術研究所饒偉研究員、國家納米科學中心王磊研究員及北京中醫藥大學東方醫院周天主任醫師為本文通訊作者。
本研究工作得到了低溫科學與技術全國重點實驗室的大力支持,團隊通過生物傳熱傳質、材料學和醫學等多學科交叉融通形成科研合力,闡明了可變形液態金屬納米顆粒“由小變大、由外入內、由靜變動”的物理化學作用機制,也為解決納米材料在單細胞中的滯留與滲透矛盾提供了全新的研究思路。
圖1.液態金屬納米顆粒介導線粒體損傷并
放大ICD、協同IRE實現腫瘤疫苗式免疫治療的總體策略
圖2. 靶向與自組裝協同提升細胞攝取并定位至溶酶體
圖3. LMPs在溶酶體內自融合增大并部分逃逸至胞質
圖4. Ga³?鐵替代導致線粒體損傷并放大ICD與先天免疫信號






所有評論僅代表網友意見,與本站立場無關。